Винникова М.А., Мохначев С.О., Ненастьева А.Ю.,
Усманова Н.Н., Козырева А.В.
ФГУ «Национальный научный центр наркологии» МЗСР РФ, г.Москва
Состояние вопроса
Проведенное на базе ННЦ наркологии в 2006 г. исследование терапевтической эффективности и безопасности применения Цианамида в комплексном лечении алкогольной зависимости в сравнении с традиционным лечением у мужчин в возрасте от 25 до 60 лет (Иванец Н.Н. и др., 2006) показало хорошую эффективность препарата на этапе формирования ремиссии. Применение Цианамида позволило значительно снизить количество ранних рецидивов и, соответственно, улучшить качество ремиссии. Цианамид хорошо сочетался с психофармакологическими и другими препаратами, не усиливая и не ослабляя их действия, не оказывал угнетающего влияния на психофизическое состояние пациентов. Прием препарата при рекомендуемом режиме дозирования не вызывал ухудшения функций печени или каких либо других значительных побочных эффектов. Цианамид существенно не влиял на динамику психопатологических, соматовегетативных и неврологических нарушений в структуре постабстинентного состояния и на этапе формирования ремиссии, однако способствовал стабилизации состояния пациентов благодаря улучшению качества ремиссий. В связи с тем, что в России применение сенсибилизирующих препаратов продолжает оставаться одним из наиболее широко распространенных при лечении больных алкогольной зависимостью, в ННЦ Наркологии проведено открытое рандомизированное клиническое исследование Цианамида в сравнении с Дисульфирамом.
Цель исследования
Изучить эффективность и безопасность применения Цианамида в комплексном лечении больных с алкогольной зависимостью в сравнении с Дисульфирамом. Будут изучены: спектр терапевтической эффективности Цианамида, его влияния на качество жизни пациентов в ремиссии, оценка приверженности проводимому лечению и анализ рецидивов заболевания в сравниваемых группах.
Материалы и методы
Общее количество больных, принимавших участие в исследовании, составило 60 человек. Они проходили стационарный курс лечения на базе стационарных отделении клиники ННЦ наркологии МЗСР РФ и амбулаторный курс лечения на базе НД №3 г. Москвы.
В начале исследования больные случайным образом делились на 2 группы – основную и контрольную, по 30 человек в группе. Все пациенты были мужского пола, в возрасте от 25 до 65 лет. Средний возраст и распределение больных по возрасту представлено в таблицах 1 и 2.
Таблица 1.
Средний возраст больных в исследуемых группах
| Средний возраст
M±m |
|
| Основная группа Цианамид (n=30) | 44,03 ± 10,17 |
| Контрольная группа Дисульфирам (n=30) | 40,47 ± 9,53 |
Таблица 2.
Распределение больных по возрасту
| Возраст,
лет |
Основная группа (Цианамид) | Контрольная группа (Дисульфирам) | ||
| Абс. число | % | Абс. число | % | |
| 25 – 30 | 3 | 10,0 | 4 | 13,3 |
| 31 – 35 | 5 | 16,7 | 9 | 30,0 |
| 36 – 40 | 4 | 13,3 | 5 | 16,7 |
| 41 – 45 | 4 | 13,3 | 2 | 6,7 |
| 46 – 50 | 5 | 16,7 | 2 | 6,7 |
| 51 – 65 | 9 | 30,0 | 8 | 26,7 |
| Всего | 30 | 100,0 | 30 | 100,0 |
Диагностика осевых синдромов зависимости проводилась по МКБ-10. Соответственно критериям включения, выборка была представлена больными со средней (II, II – III) и конечной (III) стадиями алкогольной зависимости. В основной группе у 15 пациентам была диагностирована средняя стадия и у 5 – конечная стадия зависимости от алкоголя. В контрольной группе у 16 и 4 больных соответственно.
Длительность заболевания в представленной выборке варьировала от 5 до 35 лет: средняя длительность в основной группе составила 14,77±8,18 лет; в контрольной – 12,67±6,75 лет.
Преобладающей формой злоупотребления алкоголем в обеих группах являлась псевдозапойная: она диагностировалась у 20 пациентов основной (66,7%) и у 19 пациентов контрольной групп (63,3 %) (таблица 3).
Таблица 3.
Форма злоупотребления алкоголем в группах
| Основная группа | Контрольная группа | |||
| Абс.число | % | Абс.число | % | |
| Псевдозапои | 20 | 66,7 | 19 | 63,3 |
| Постоянная на фоне высокой толерантности | 9 | 30,0 | 9 | 30,0 |
| Постоянная на фоне низкой толерантности | 1 | 3,3 | 1 | 3,3 |
| Перемежающаяся | 0 | 0 | 1 | 3,3 |
| Истинные запои | 0 | 0 | 0 | 0 |
| Всего | 30 | 100,0 | 30 | 100,0 |
У большинства пациентов (по 21 человеку в основной и контрольной группах – 70%) темп прогредиентности заболевания был квалифицирован как средний. В остальных случаях темп заболевания был высокопрогредиентным, у 1 пациента контрольной группы – низким.
Толерантность на момент обследования составляла в среднем от 0,3 до 1,5 л крепких спиртных напитков в сутки (таблица 4).
Таблица 4.
Уровень толерантности в исследуемых группах.
| Толерантность (мл) | |
| Всего | 844,2±330,0 |
| Основная группа (n=30) | 790,0±344,8 |
| Контрольная группа (n=30) | 898,3±310,9 |
Алкогольные изменения личности диагностировались у большинства пациентов (у 27 пациентов основной и у 28 контрольной групп, в 90,0% и 93,3% соответственно). Социальные последствия алкогольной зависимости (потеря работы, конфликты в семье, развод и т.д.) также имели место в большинстве случаев: у 26 пациентов основной и у 27 – контрольной групп (86,7% и 90,0%, соответственно), отсутствовали у 4 человек в основной группе и у 3 в контрольной (13,3% и 10,0%).
ААС протекал с типичными для него соматовегетативными, неврологическими и психопатологическими расстройствами. Длительность абстинентного синдрома составляла от 5 до 12 дней. Соматовегетативные нарушения были представлены гипергидрозом, бледностью или гиперемией лица, жаждой, диспепсическими нарушениями, болями в области сердца, колебаниями АД, тахикардией, в ряде случаев – субфебрильным повышением температуры тела. Из аффективных расстройств преобладали снижение настроения, раздражительность, тревога, внутреннее напряжение, эксплозивность, эмоциональная лабильность, чувство вины, нарушения сна. Неврологические расстройства проявлялись генерализованным тремором, нистагмом, нарушениями при выполнении координационных проб, шаткостью походки. У части больных не удалось выделить ведущий компонент в структуре ААС из-за одинаковой по силе выраженности расстройств разных кластеров (таблица 5).
Таблица 5.
Преобладающая симптоматика в ААС
| Основная группа (n=30) | Контрольная группа (n=30) | |
| С астеновегетативными
расстройствами |
2 (6,7%) | 1 (3,3%) |
| С преобладанием неврологических и соматовегетативных расстройств | 28 (93,3%) | 29 (96,7%) |
| С преобладанием психических расстройств: | 12 (40%) | 12 (40%) |
| Снижение настроения с оттенком тревоги | 7 (23,3%) | 9 (30%) |
| Дисфория, раздражительность, эксплозивность | 5 (16,7%) | 1 (3,3%) |
| С обратимыми психоорганическими расстройствами | 0 (0%) | 2 (6,7%) |
У всех больных имелись соматические заболевания, обусловленные длительной интоксикацией алкоголем (вне обострения): чаще других диагностировались алкогольная болезнь печени (хронический токсический стеатогепатит), миокардиодистрофия, артериальная гипертензия. У многих больных выявлялись признаки энцефалопатии, в основном средней степени тяжести, чаще токсического генеза.
Таким образом, по возрастным, основным социально-демографическим и клинико-динамическим показателям группы практически не различались.
В постабстинентном состоянии (период после купирования ААС до 3 – 4-х недель воздержания от употребления алкоголя) наиболее частыми были астенические проявления (повышенная утомляемость, вялость, снижение работоспособности). Имели место также различные аффективные нарушения: сниженный фон настроения, тревожность, раздражительность, дисфория, склонность к частой смене настроения, связанные, чаще всего, с обострением патологического влечения к алкоголю. Сохранялись мнестические нарушения, вегетативная дисфункция, расстройства сна (трудности засыпания, поверхностный сон, частые пробуждения).
Этап становления ремиссии (от 4-х недель до 6-х месяцев применительно к данному исследованию) диагностировался при условии, что больной в течение наблюдаемого периода времени полностью воздерживается от употребления алкоголя и других психоактивных веществ.
Основными методами исследования являлись клинико-психопатологический, катамнестический, статистический.
Клиническое исследование Цианамида проводилось с использованием специально разработанного протокола, максимально отвечающего международным требованиям GCP (качественной клинической практики). Протокол включал сведения о социальном статусе больных, клинико-динамических характеристиках заболевания, результатах обследования физического и психического состояния, данных лабораторных анализов в динамике, результатов опросников и шкал. Подробно были представлены сведения об объеме проводимой терапии. Проводился количественный анализ рецидивов.
При оценке спектра терапевтической активности препарата использовались специально разработанные в ННЦ наркологии шкалы динамики психопатологических, астенических и астенодепрессивных расстройств в абстинентном состоянии, в постабстинентном периоде, на этапе формирования ремиссии. Оценка состояния по данным шкалам производилась по 4-х бальной системе, где 0 баллов – отсутствие симптома, 1 – слабо выраженный, 2 – средне выраженный и 3 – значительно выраженный. Различия средних величин, а также корреляционные связи признавались достоверными при уровне значимости p<0,05. Для оценки динамики состояния пациентов использовалась шкала общего клинического впечатления.
По модифицированной шкале оценки побочных эффектов UKU на всем протяжении лечения оценивались побочные явления терапии. Отмечались сведения о нежелательных явлениях (шкала оценки наличия и выраженности нежелательных явлений): характере, времени возникновения и прекращения нежелательных явлений, их тяжести, связи с исследуемым препаратом, являлись ли нежелательные явления серьезными, а также меры, предпринятые для их устранения.
Оценка тяжести депрессии, отслеживания ее динамики в процессе терапии проводилась по Шкале Монтгомери-Асберг (MADRS). Эффективность терапии считают удовлетворительной, если к моменту окончания лечения суммарный балл снижается как минимум на 50% от начального.
Для оценки показателей качества жизни пациентов использовался опросник SF-36 (Health status profile – Shot form 36).
Оценка приверженности (комплайенса) противоалкогольному лечению производилась по 4-х бальной системе, где 0 баллов – отсутствие комплайенса, 1 – низкий комплайенс, 2 – средний комплайенс и 3 – сильный комплайенс.
Оценка безопасности действия препарата производилась с учетом динамики лабораторных показателей (АЛТ, АСТ, ГГТ).
При проведении статистической обработки материала использовались количественные и качественные показатели, рассчитывалась достоверность результатов исследования. В связи с поставленными задачами проводилось внутригрупповое и межгрупповое сравнение. Описательный статистический анализ проводился с применением программы Excel 2000. Для установления статистической достоверности различий между группами использовался параметрический показатель t-критерия Стьюдента для количественных показателей с применением программ Statistica 5.5. и SPSS 10.0. При анализе межгрупповых различий показателей статистически значимым считался р<0,05.
Пациенты, соответствующие критериям включения в исследование в основной группе получали ежедневно Цианамид по 30 мг (10 капель) дважды в сутки внутрь в течение 24 недель (168 дней).
Пациенты, соответствующие критериям включения в исследование в контрольной группе получали Дисульфирам по 150 мг дважды в сутки внутрь в течение 24 недель.
Лечение ААС в группах было комплексным и включало проведение стандартных дезинтоксикационных мероприятий. В последующем случае выраженных аффективных и поведенческих нарушений пациентам назначалась дополнительная терапия. Все дополнительные лекарственные препараты фиксировались в Индивидуальной Регистрационной Карте (ИРК) в разделе сопутствующей терапии. Терапевтические схемы были максимально стандартизованы, не отличались по своим подходам в основной и контрольной группах. Различия наблюдались лишь в индивидуальных дозах назначаемых препаратов.
При выборе нейролептика предпочтение отдавалось малым дозам нейролептиков-антипсихотиков (галоперидол до 10 мг, трифтазин до 15 мг, этаперазин до 40 мг, рисполепт до 4 мг), в вечернее время назначались (короткими курсами) препараты с седативным действием (неулептил до 30 мг, сонапакс до 50 мг). Назначение нейролептических препаратов всякий раз тщательно обосновывалось и производилось лишь в тех случаях, когда избежать их использования в терапевтических программах не представлялось возможным. Кроме того, все пациенты получали терапию ноотропами, витаминами, гепатотропами. На всем протяжении стационарного лечения проводилась индивидуальная рациональная психотерапия. В обеих группах не проводились психотерапевтические «запретительные» процедуры.
Результаты исследования
Преждевременное прекращение участия в исследовании происходило в основном по причинам не связанным с исследуемой терапией: появление у пациента критериев исключения во время проведения исследования, серьезное отклонение от протокола исследования, желание пациента выйти из исследования. Пациенты также исключались из исследования, если пропускали более 4-х приемов исследуемого препарата подряд, или суммарно в течение месяца более 10% всей дозы.
По причинам, связанным с исследуемой терапией (серьезные нежелательные явления или значительные отклонения в лабораторных анализах, требующие отмены исследуемой терапии) преждевременного завершения исследования не наблюдалось (таблица 6).
Таблица 6.
Причины преждевременного завершения исследования
| Группа | Причина выхода из исследования | Абсолютное число |
| Основная группа (Цианамид) | Актуализация ПВА, возобновление приема алкоголя | 6 |
| Пропуск более 4-х приемов исследуемого препарата подряд | 2 | |
| Контрольная группа (Дисульфирам) | Актуализация ПВА, возобновление приема алкоголя | 8 |
| Пропуск более 4-х приемов исследуемого препарата подряд | 4 | |
| Всего: | 20 пациентов | |
Как показывают данные таблицы 13, из основной группы выбыло 8 пациентов (26%), в то время как из контрольной группы выбыло 12 пациентов (40%). При этом следует обратить внимание на тот факт, что по причине несоблюдения режима терапии из контрольной группы выбыло в 2 раза больше пациентов.
Остальные пациенты, 74% в основной группе и 60% в контрольной группе прошли весь период терапии без срывов и рецидивов. Формирование ремиссии в течение 6 месяцев у выше указанного количества пациентов является хорошим результатом. Однако, следует обратить внимание на более оптимистичный результат в группе получавшей Цианамид по сравнению с группой получавшей Дисульфирам.
В дальнейшей работе анализ проводился по тем пациентам, которые полностью прошли весь курс терапии.
В исследовании участвовали больные, изначально мотивированные на лечение, как в основной, так и в контрольной группе. Комплайенс при поступлении на лечение был в пределах 1,8-1,9 баллов, что соответствует среднему уровню. В процессе терапии наблюдалась интересная динамика данного показателя в группах. Отсутствие динамики или даже его небольшое снижение комплайенса наблюдалось в первую-вторую неделю терапии (до 3-го визита, 14-й день).
К концу первого месяца терапии (6-й визит, 28-й день) в основной группе показатель комплайенса увеличился (до 2,5 баллов), в то время как в группе контроля он оставался практически прежним (не достигал 2-х баллов).
Через 6 месяцев терапии в основной группе данный показатель колебался в пределах 2,5 баллов (оценка комплайенса – от среднего до высокого); в группе же контроля этот показатель достиг только уровня 2-х баллов (средний уровень) (рисунок 1).
Рисунок 1.
Комплайенс в группах сравнения
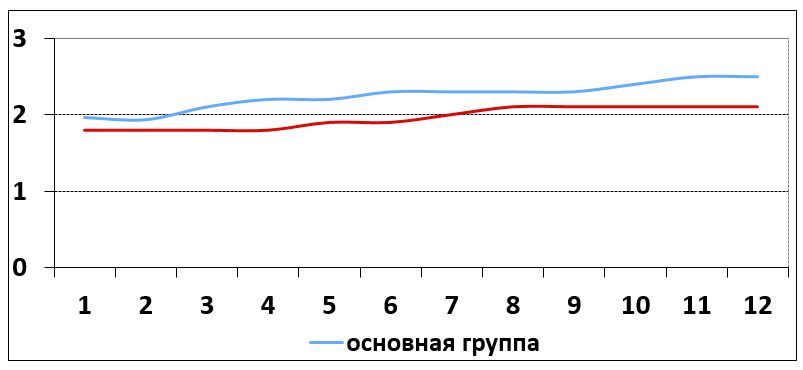
Таким образом, наглядно видно, что при равных условиях начала терапии, в основной группе наблюдается более выраженный рост комплайенса в динамике лечения по сравнению с контрольной группой. Несмотря на то, что статистически достоверной разницы между группами достигнуто не было, те не менее, данную тенденцию важно учитывать при составлении терапевтической программы для больного алкогольной зависимостью.
Оценка динамики психопатологических нарушений у пациентов основной и контрольной групп выявила достоверное снижение степени их выраженности внутри групп в результате проводимого комплексного лечения.
Достаточно интересные данные получены при сравнении динамики патологического влечения к алкоголю в группах (таблица 7). Как видно из таблицы 7, изначально в контрольной группе уровень влечения к алкоголю был несколько выше (хотя достоверных различий с основной группой не было). Тем не менее, в группе контроля уровень влечения достоверно снижался к 14-му дню терапии, а в основной группе – к 28-му дню лечения. Данный факт, несомненно, имеет обоснование. Хорошо известно, что дисульфирам тормозит один из важнейших ферментов синтеза катехоламинов – дофамин-β-карбоксилазу, тем самым, снижая уровень дофамина в крови. При этом, Цианамид не влияет на активность дофамин-β-карбоксилазы, а соответственно, и на метаболизм катехоламинов.
По всей видимости, за счет данного механизма и происходит более быстрое купирование синдрома патологического влечения к алкоголю в контрольной группе.
Учитывая то, что терапия в группах была минимизирована и стандартизирована, можно говорить о том, что полученный результат достоверен.
Таблица 7.
| Визит 2
Начало исследования |
Визит 4
14-й день |
Визит 6
28-й день |
Визит 8
56-й день |
Визит 10
84-й день |
Визит 11
112-й день |
Визит 12
140-й день |
Визит 13
168-й день |
|
| Осн группа (Цианамид) | 1,8
±0,89 |
1,47
±0,82 |
1,24
±0,64 (*) |
0,92
±0,8 |
0,39
±0,58 |
0,05
±0,21 |
0,05
±0,21 |
0,14
±0,35 |
| Контроль
(Дисульфирам) |
2,07
±0,58 |
1,47
±0,63 (**) |
1,17
±0,59 |
0,83
±0,56 |
0,41
±0,67 |
0,11
±0,32 |
0
±0,0 |
0,06
±0,24 |
Примечание:
* – различия достоверны для уровня значимости р<0,01 (внутригрупповое сравнение).
** – различия достоверны для уровня значимости р<0,001 (внутригрупповое сравнение).
Не менее интересными получились данные при анализе динамики психопатологических нарушений (таблица 8). В основной группе достоверно быстрее купировались такие расстройства, как подавленность, заторможенность, расстройства сна, раздражительность и неустойчивость внимания. Особое внимание необходимо обратить на сравнительно быстрое купирование расстройств сна в основной группе, которое происходило ко второй неделе терапии. Более быстрое купирование подавленности, заторможенности, раздражительности и неустойчивости внимания в основной группе можно связать с более быстрой стабилизацией физического здоровья пациентов.
Таблица 8.
Динамика психопатологической симптоматики в группах
| Симптомы | Дни исследования | Основная группа
Цианамид |
Контрольная группа
Дисульфирам |
| Моторное возбуждение, ажитация | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,5±0,68
0,23±0,43 0,1±0,31 0,04±0,2 0 0 0 0 |
0,8±0,81
0,47±0,63 0,1±0,31 0,13±0,34 0 0 0 0 |
| Напряженность | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
1,4±0,77
0,9±0,61 0,52±0,57 0,31±0,47 0,13±0,34 0,05±0,21 0,14±0,35 0,23±0,43 |
1,57±0,68
1,07±0,64 0,57±0,57 0,5±0,59 0,27±0,46 0,05±0,22 0 0,05±0,23 |
| Тревожность | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
1,77±0,77
1,03±0,72 0,79±0,56 0,46±0,51 0,09±0,29 0,05±0,21 0,05±0,21 0,18±0,39 |
1,67±0,66
1,03±0,72 0,8±0,66 0,5±0,59 0,18±0,39 0,11±0,32 0,06±0,24 0,17±0,38 |
| Дисфория | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,3±0,65
0,23±0,57 0,03±0,19 0,04±0,2 0 0 0 0 |
0,27±0,64
0,1±0,4 0,07±0,37 0,04±0,2 0,09±0,29 0 0 0 |
| Подавленность | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
1,53±0,73
1,1±0,76 0,76±0,51 0,35±0,49 0,09±0,29 0,05±0,21* 0 0,05±0,21 |
1,73±0,74
1,3±0,7 0,77±0,68 0,54±0,51 0,27±0,46 0,32±0,48* 0,06±0,24 0,11±0,32 |
| Эмоциональная лабильность | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
1,2±0,71
0,77±0,68 0,41±0,63 0,04±0,2 0,09±0,29 0 0 0,05±0,21 |
1,37±0,72
0,77±0,57 0,37±0,49 0,08±0,28 0,05±0,21 0,05±0,22 0 0,06±0,24 |
| Заторможенность | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,5±0,57
0,2±0,48 0,03±0,19* 0,04±0,2 0 0 0 0 |
0,8±0,76
0,4±0,62 0,23±0,43* 0,13±0,34 0,05±0,21 0,05±0,23 0,06±0,24 0,06±0,24 |
| Расстройства сна | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,93±0,69**
0,6±0,56** 0,14±0,35** 0* 0 0 0 0 |
1,73±0,78**
1,1±0,66** 0,5±0,51** 0,21±0,41* 0,14±0,35 0,05±0,23 0 0 |
| Чувство вины | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
1,03±1,0
0,63±0,72 0,28±0,45 0,08±0,27 0 0 0,05±0,21 0 |
1,23±0,82
0,7±0,6 0,4±0,56 0,08±0,28 0,05±0,21 0,05±0,23 0,06±0,24 0 |
| Истощаемость | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,83±0,83
0,43±0,57 0,14±0,35 0,08±0,27 0 0 0 0 |
1,03±0,72
0,6±0,56 0,33±0,48 0,25±0,44 0,14±0,35 0,11±0,32 0,06±0,24 0 |
| Повышенная раздражительность | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,63±0,67
0,27±0,52 0,1±0,31* 0,15±0,37 0,04±0,21 0 0 0,05±0,21 |
0,97±0,89
0,57±0,68 0,33±0,55* 0,13±0,34 0,05±0,21 0,11±0,32 0 0,06±0,24 |
| Неустойчивость внимания | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
0,8±0,66*
0,5±0,57 0,14±0,35* 0,08±0,27 0,09±0,29 0 0 0 |
1,13±0,51*
0,7±0,6 0,37±0,49* 0,17±0,38 0,09±0,29 0 0 0 |
| Пониженный фон настроения | 0 день
14 день 28 день 56 день 84 день 112 день 140 день 168 день |
1,87±0,51
1,33±0,55 0,9±0,67 0,54±0,51 0,13±0,34 0,05±0,21 0,05±0,21 0,05±0,21 |
2,0±0,59
1,33±0,48 1,03±0,56 0,71±0,55 0,32±0,57 0,25±0,44 0,11±0,32 0,06±0,24 |
Примечание:
* – различия достоверны для уровня значимости р<0,05 (межгрупповое сравнение).
** – различия достоверны для уровня значимости р<0,001 (межгрупповое сравнение).
Оценка динамики аффективных нарушений по шкале Монтгомери-Асберг у пациентов основной и контрольной групп также выявила достоверное снижение степени их выраженности внутри групп в результате проводимого комплексного лечения. Между группами наблюдались достоверные различия в динамике таких расстройств как подавленность, внутреннее напряжение, нарушение сна, нарушение внимания, наличие пессимистических мыслей и по общему баллу депрессивных расстройств (таблица 9).
Таблица 9.
| Симптомы | День исследования | Основная группа
Цианамид |
Контрольная группа
Дисульфирам |
| Признаки подавленности | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
1,57±0,57
0,86±0,35* 0,62±0,5 0,21±0,41 0 0 0 |
1,8±0,61
1,1±0,48* 0,67±0,56 0,32±0,57 0,16±0,37 0,06±0,24 0 |
| Высказывания о подавленности | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
1,27±0,69
0,9±0,49 0,5±0,51 0,04±0,21* 0,05±0,21 0 0 |
1,43±0,68
1,0±0,59 0,63±0,58 0,41±0,67* 0,16±0,37 0,06±0,24 0 |
| Внутреннее напряжение | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
1,37±0,61
0,9±0,67* 0,27±0,45 0,22±0,42 0,05±0,21 0,14±0,35 0 |
1,57±0,68
0,57±0,57* 0,5±0,59 0,27±0,46 0,11±0,32 0 0,06±0,24 |
| Ухудшение сна | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
0,97±0,67**
0,21±0,41* 0,04±0,2 0 0 0 0 |
1,73±0,78**
0,5±0,51* 0,17±0,38 0,14±0,35 0,05±0,23 0 0,06±0,24 |
| Нарушение аппетита | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
0,07±0,25
0 0 0 0 0 0 |
0,13±0,35
0 0 0 0 0 0,05±0,23 |
| Нарушение внимания | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
0,8±0,66*
0,14±0,35* 0,08±0,27 0,05±0,21 0±0,0 0 0 |
1,13±0,51*
0,4±0,5* 0,17±0,38 0,09±0,29 0 0 0 |
| Нарушение интенции деятельности | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
1,13±0,68
0,32±0,48 0,08±0,28 0 0 0 0 |
1,03±0,72
0,33±0,48 0,21±0,41 0,09±0,29 0,11±0,32 0 0 |
| Утрата чувств | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
0,73±0,83
0,28±0,45 0,04±0,2 0 0 0,05±0,22 0,05±0,22 |
0,9±0,8
0,23±0,43 0,08±0,27 0,05±0,21 0,05±0,23 0,06±0,24 0 |
| Пессимистические мысли | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
0,73±0,69*
0,24±0,44 0,08±0,27 0 0 0 0,05±0,21 |
1,2±0,81*
0,37±0,49 0,04±0,2 0 0 0 0 |
| Суицидальные мысли | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
0
0 0 0 0 0 0 |
0,03±0,18
0 0 0 0 0 0 |
| Общий балл по шкале Монтгомери-Асберг | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
8,63±3,25*
3,83±2,19 1,69±1,52 0,52±0,9 0,09±0,42 0,18±0,5 0,09±0,43 |
10,97± 3,84*
4,5±2,65 1,97±2,04 1,0±1,74 0,4±1,0 0,1±0,31 0,1±0,4 |
Примечание:
* – различия достоверны для уровня значимости р<0,05 (межгрупповое сравнение).
** – различия достоверны для уровня значимости р<0,001 (межгрупповое сравнение).
В ходе исследования выявлена достоверно положительная динамика по всем осям шкалы КЖ пациентов (таблица 10).
Таблица 10.
Динамика показателей качества жизни по шкале SF-36
| Оси
шкалы SF-36 |
Дни исследования | Основная группа
Цианамид |
Контрольная группа
Дисульфирам |
| Физическое функционирование | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
89,8±7,13*
91,6±7,7 94,8±6,7 96,7±4,91 97,0±5,04 97,7±4,29 98,2±3,29 |
84,2±14,1*
88,0±11,0 91,0±8,7 94,3±9,08 97,5±4,7 98,1±4,25 97,5±4,3 |
| Ролевое функционирование, обусловленное физическим состоянием | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
62,5±30,62
69,0±33,84 89,4±18,9 91,3±22,0 93,2±22,07 93,2±22,1 94,3±21,7 |
59,2±27,0
74,2±23,0 84,4±16,0 85,9±20,0 91,3±15,0 93,1±12,0 93,1±12,0 |
| Интенсивность боли | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
74,0±24,0
85,0±19,0 94,7±12,0 94,9±13,6 96,6±13,0 98,3±8,1 98,8±5,54 |
74,5±20,0
81,8±17,0 90,5±13,0 93,5±11,9 97,4±6,4 96,2±7,32 98,0±5,9 |
| Общее состояние здоровья | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
70,2±18,6
78,0±20,0 85,2±17,6 90,0±16,0 88,95±16,98 91,0±15,0 91,9±13,1 |
70,0±17,0
80,1±15,0 85,4±12,0 89,6±9,5 92,1±6,24 93,72±4,8 94,6±3,4 |
| Жизненная активность | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
62,8±17,2
73,3±17,3 85,0±13,2 87,8±13,9 88,0±12,0 89,0±13,0 90,0±13,0 |
70,2±17,2
80,0±14,0 84,2±11,9 87,5±9,73 88,4±6,68 90,1±4,67 90,8±4,62 |
| Социальное функционирование | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
58,3±24,4
75,0±20,0 82,0±14,5 84,2±12,6 84,7±11,5 84,0±11,0 85,0±11,0 |
60,0±18,0
72,1±17,0 79,7±13,7 83,0±9,9 85,5±4,68 86,1±4,04 86,8±2,95 |
| Ролевое функционирование, обусловленное эмоциональным состоянием | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
52,0±26,0*
62,2±22,7* 69,0±13,0* 66,7±10,1 67,0±18,0 71,2±21,3 77,3±23,9 |
33,0±23,0*
49,0±19,0* 57,0±15,5* 65,2±7,1 68,4±7,6 66,7±0,1 72,2±12,8 |
| Психическое здоровье | 0 день
28 день 56 день 84 день 112 день 140 день 168 день |
53,9±15,6
65,9±16,0 77,1±10,9 80,2±11,3 84,5±14,0 87,8±13,0 88,9±15,0 |
56,7±18,3
65,1±16,0 72,0±12,0 79,0±11,0 83,8±10,9 86,9±8,98 88,9±7,2 |
Примечание:
* – различия достоверны для уровня значимости р<0,05 (межгрупповое сравнение).
При сравнении показателей КЖ между группами, достоверно быстрее в основной группе восстанавливалось ролевое функционирование, обусловленное эмоциональным состоянием.
По остальным показателям достоверных различий получено не было. Однако следует отметить тенденцию более быстрого улучшения показателей КЖ в основной группе по сравнению с контрольной при их стремлении практически к норме в течение полугода терапии. Речь идет о физическом функционировании, общем состоянии здоровья, жизненной активности. Показатели социального функционирования и психического здоровья восстанавливались в группах медленнее. Полученные результаты по шкале КЖ имеют большое значение для оценки стабильности ремиссии в целом, а также для определения длительности проводимой терапии. То есть, опираясь на полученный результат, можно говорить о том, что в отношении стабилизации психического состояния и социального функционирования требуется продолжение терапии более полугода.
Одной из основных задач исследования являлось определение безопасности использования Цианамида длительно, в течение 6 месяцев (полугода) постоянного приема.
Оценка безопасности применения Цианамида проводилась по динамике лабораторных показателей в группах (таблица 11). Данные таблицы 11 наглядно показывают, что пациенты поступали на лечение с показателями токсического поражения печени (АЛТ, АСТ, ГГТ), превышающими норму в 2-3 раза. По окончании терапевтической программы эти показатели стремились к норме. При этом следует отметить выраженную тенденцию к улучшению печеночных функций в основной группе: показатели АЛТ, АСТ в конце лечения являются практически нормой, в то время как в контрольной группе они значительно выше нормы (рисунок 2-4).
Отметим, что ГГТ превышает показатель нормы в двух группах. Однако в группе контроля это превышение практически в два раза, в то время как в основной группе только в полтора раза
Таблица 11.
Динамика лабораторных показателей в группах сравнения
| ферменты | Дни исследования | Основная группа
Цианамид |
Контрольная группа
Дисульфирам |
| АЛТ | 0
168 |
86,4±55,33
47,5±20,3 |
89,73±68,36
58,78±16,09 |
| АСТ | 0
168 |
89,97±68,93
42,6±17,03 |
94,82±73,1
50,72±17,52 |
| ГГТ | 0
168 |
138,2±92,73
69,37±29,36 |
137,4±121,45
85,39±58,07 |
Рисунок 2.
Динамика АЛТ в группах в сравнении
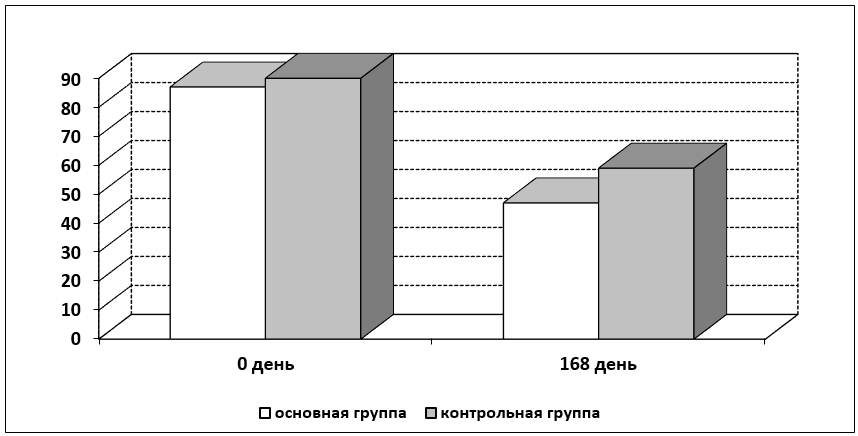
Примечание: Через 6 месяцев терапии показатель АЛТ достигает нормы в основной группе. В контрольной группе имеется тенденция к улучшению, но значения нормы показатель не достигает.
Рисунок 3.
Динамика АСТ в группах в сравнении
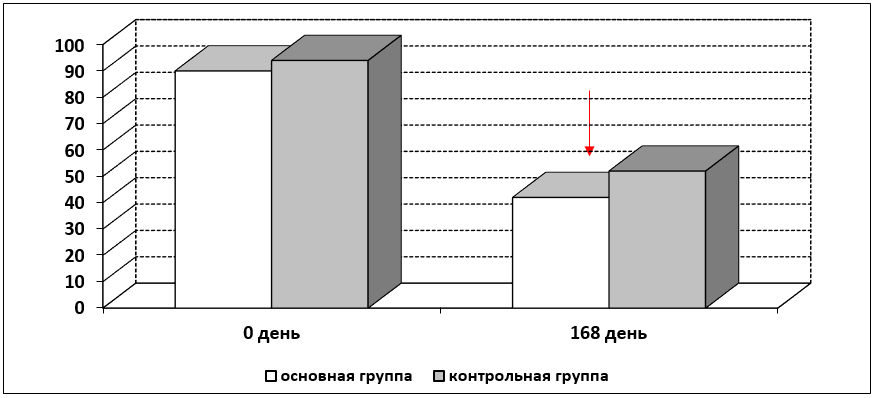
Примечание: Практически идентичный результат: через 6 месяцев терапии показатель АСТ достигает нормы в основной группе. В контрольной группе имеется тенденция к улучшению, но значения нормы показатель не достигает.
Рисунок 4.
Динамика ГГТ в группах в сравнении
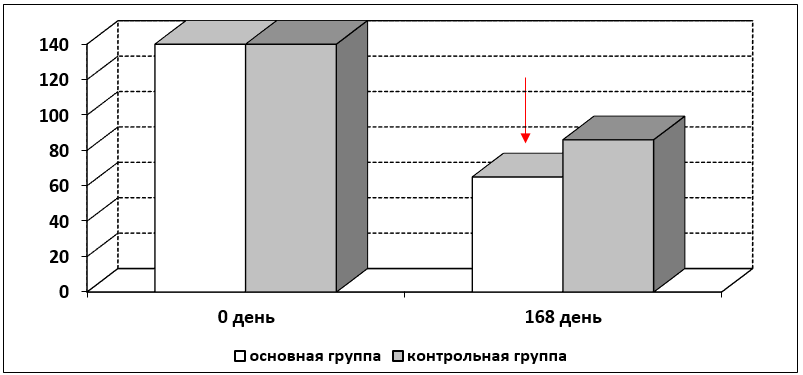
Примечание: Рисунок наглядно показывает, что при поступлении на лечение показатель ГГТ в группах достаточно высок, превышает норму более, чем в 3 раза, что является признаком острой интоксикации. Через 6 месяцев лечения в основной группе показатель стремится к норме, в контрольной же группе этот показатель выше нормы более чем в 2 раза.
Заключение
Цианамид проявил себя как препарат с высокой эффективностью и безопасностью, даже при длительном (6 месяцев) постоянном приеме.
Формирование ремиссии в процессе проведения исследования было достигнуто у 76% пациентов, получавших Цианамид по сравнению с 60% пациентов, получавших Дисульфирам.
У пациентов, получавших Цианамид, наблюдался более выраженный рост комплайенса в динамике лечения по сравнению с группой, получавшей Дисульфирам. Полученные данные важно учитывать при составлении терапевтической программы для больного алкогольной зависимостью.
При сравнении динамики патологического влечения к алкоголю было выявлено, что в группе пациентов, получавших Дисульфирам, редукция патологического влечения происходит быстрее по сравнению с группой пациентов, получавших Цианамид. Это связано с отличиями в механизме действия двух лекарств на дофаминовую систему.
Были получены интересные данные при анализе динамики психопатологических, в том числе аффективных нарушений. В группе пациентов, получавших Цианамид, достоверно быстрее купировались такие расстройства, как подавленность, заторможенность, расстройства сна, раздражительность, неустойчивость внимания и общий балл депрессивных расстройств по сравнению с группой пациентов, получавших Дисульфирам. Более быстрое купирование выше описанной симптоматики в основной группе можно связать с более быстрой стабилизацией физического здоровья пациентов.
При сравнении показателей КЖ между группами, достоверно быстрее в группе, получавшей Цианамид, восстанавливалось ролевое функционирование, обусловленное эмоциональным состоянием, по сравнению с группой, получавшей Дисульфирам.
Отмечалась выраженная тенденция улучшения показателей КЖ в группе, получавшей Цианамид, по сравнению с группой, получавшей Дисульфирам, при их стремлении к норме в течение полугода терапии. Речь идет о физическом функционировании, общем состоянии здоровья, жизненной активности. Показатели социального функционирования и психического здоровья восстанавливались в группах медленнее. Полученные результаты по шкале КЖ имеют большое значение для оценки стабильности ремиссии в целом, а также для определения длительности проводимой терапии.
Оценка безопасности применения Цианамида показала, что Цианамид не влияет в значительной степени на функцию печени. Это проявлялось в улучшении печеночных функций под действием препарата. При этом, лабораторные показатели в группе, получавшей Цианамид, лучше, чем таковые в группе, получавшей Дисульфирам. Нежелательных явлений, побочных эффектов и осложнений на фоне лечения Цианамида не было. Данные факты подтверждают безопасность препарата.
Таким образом, проведенной исследование еще раз подтвердило перспективность использования Цианамида в длительных комплексных программах терапии больных зависимостью от алкоголя.
Литература
- Алкоголизм: (Руководство для врачей)/ Под ред. Г.В. Морозова, В.Е. Рожнова, Э.А. Бабаяна. М.: Медицина. 1983.
- Валентик Ю.В., Новиков Е.М. Применение препарата Цианамид при лечении больных алкоголизмом// Наркология. 2002. № 3.
- Ерышев О.Ф., Рыбакова Т.Г. Дифференцированные методы психофармакотерапии больных алкоголизмом. //Методич. Рекоменд.: – Ленингр. НИПИ им. В.П. Бехтерева. – 1990. – 16 с.
- Ерышев О.Ф., Рыбакова Т.Г. Динамика ремиссий при алкоголизме и противорецидивное лечение. СПб.: ПНИИ им. В.М. Бехтерева, 1996. 190 с.
- Ерышев О.Ф. Этапы течения ремиссий при алкоголизме и профилактика рецидивов. Дисс. … д.м.н. в виде научного доклада: СПб. 1998. 58 с.
- Ерышев О.Ф., Рыбакова Т.Г., Шабанов П.Д. Рук-во для врачей: Алкогольная зависимость (формирование, течение, противорецидивная терапия). – С-Пб. – ЭЛБИ-СПб. – 2002. – с.4-37, 98-102, 103-147, 154-168.
- Зеневич Г.В. Ремиссии при шизофрении. М. – Медгиз. – 1964. – 268 с.
- Иванец Н.Н., Кинкулькина М.А. Новые данные о сенсибилизирующей терапии алкогольной зависимости // Журнал неврологии и психиатрии им. С.С. Корсакова. 2004. №7. С. 43-48.
- Иванец Н.Н., Винникова М.А., Козырева А.В. Результаты клинико-катамнестического сравнительного исследования препарата Цианамид в терапии алкогольной зависимости// Вопросы наркологии. 2006, № 2, С. 21 – 29.
- Ajima M., Usuki K., Igarashi A., Okazaki R., Hamano K., Urabe A. and Totsuka Y. Cyanamide-induced granulocytopenia// Internal Medicine. – 1997. – V. 36. – P. 640–642.
- Burst J.C.M. Neurological aspects of substance abuse. 2-nd Ed. Philadelphia, Elsevier Inc. 2004.
- Foster J. H., Peters T. J., Marshall E. J. Quality of life measures and outcome in alcohol-dependent men and women. //Alcohol. – 2000. – Vol. 22, № 1. – P. 45–52.
- Foster J.H., Marshall E.J., Peters T.J. Application of a quality of life measure, the life situation survey (LSS), to alcohol-dependent subjects in relapse and remission. //Alcohol. Clin. Exp. Res. – 2000. – Vol. 24, № 11. – P. 1687–1692.
- Rudolf H., Priebe S. Similarities and differences in subjective quality of life of alcoholic women // Psychiatrische Praxis. — 1999. — Vol. 266, № 3. — P. 116.
- Rudolf H., Priebe S. Subjective quality of life and depressive symptoms in women with alcoholism during detoxification treatment // Drug Alcohol Depend. — 2002. — Vol. 66, № 1. — P. 71–76.
- Suzuki Y., Yokoyama A., Nakano M., Okuyama K., Takahashi H., Tamai H., Maruyama K. and Ishii H. Cyanamide-induced liver dysfunction after abstinence in alcoholics: a long-term follow-up study on four cases// Alcoholism: Clinical and Experimental Research. – 2000. – V. 24. – P. 100S–105S.
- Swift R.M., Flannery B., Roberts A.J., Cooney N., Anton R., Rohsenow D. (2001). The role of craving in alcohol use, dependence, and treatment. Alcohol Clin Exp Res, 25(2), 299-308.
- Swift R. M. Лекарственная терапия алкогольной зависимости // Обзор современной психиатрии. — 2001. — Вып. 3. — С. 61–70.
- Tamai H., Yokoyama A., Okuyama K., Takahashi H., Maruyama K., Suzuki Y. and Ishii H. Comparison of cyanamide and disulfiram in effects on liver function. Alcoholism: Clinical and Experimental Research. – 2000. – V. 24. – P. 97S–99S.
- Yokoyama A., Sato S., Maruyama K., Nakano M., Takahashi H., Okuyama K., Takagi T., Yokoyama T. and Hayashida M. (1995) Cyanamide-associated alcoholic liver disease: a sequential histological evaluation. Alcoholism: Clinical and Experimental Research 19, 1307–1311.
- Yerro C.P., Lopez C.P., Bernardino, A.R., Martinez R.M., delPorto-Gomez, E. and Carmona A..A. Relapsing pancytopenia following exposure and re-exposure to cyanamide// European Journal of Haematology. – 2000. – V. 65. – P. 414–415.





