Иванец Н.Н., Винникова М.А., Козырева А.В.
Национальный научный центр наркологии, г. Москва
Цель и задачи исследования
Изучить терапевтическую эффективность и безопасность применения Цианамида в комплексном лечении алкогольной зависимости в сравнении с традиционным лечением.
Материал и методы исследования
Общее количество больных, принимавших участие в исследовании, составило 60 человек, проходивших стационарный курс лечения в клинике ННЦ наркологии.
В начале исследования больные случайным образом делились на 2 группы – основную (32 чел.) и контрольную (28 чел.). Все пациенты были мужского пола, в возрасте от 25 до 60 лет, средний возраст больных в основной группе составил 41,63±1,35 года, в контрольной – 38,82±1,87.
Большинство больных в обеих группах (75,00 % в основной и 71,43 % в контрольной) имели наследственную отягощенность наркологическими заболеваниями, при этом значительно чаще встречался алкоголизм отца или родственников по отцовской линии.
В обеих группах преобладали работающие лица (75,00 % в основной и 57,14% в контрольной), из них основная часть занималась физическим трудом.
Диагностика осевых синдромов зависимости проводилась согласно диагностическим критериям МКБ-10. Соответственно критериям включения, выборка была представлена больными со средней (II, II–III) и конечной (III) стадиями алкогольной зависимости. Длительность заболевания в представленной выборке варьировала от 5 до 40 лет, средняя его длительность в основной группе составила 19,13±1,20, в контрольной – 15,86±1,69 лет. Преобладающей формой злоупотребления алкоголем в обеих группах являлась псевдозапойная: у 14 пациентов основной (43,75%) и у 14 пациентов контрольной групп (50,00 %)
У большинства пациентов (18 человек основной группы и 18 контрольной, 56,25% и 64,29%, соответственно) темп прогредиентности заболевания был квалифицирован как средний. В остальных случаях темп заболевания был высокопрогредиентным, у 1 пациента контрольной группы – низким. Толерантность на момент обследования составляла в среднем от 0,5 до 2 л крепких спиртных напитков. ААС протекал с типичными для него соматовегетативными, неврологическими и психопатологическими расстройствами. Степень тяжести ААС в большинстве случаев была квалифицирована как средняя (20 пациентов основной группы и 24 контрольной – 62,50 % и 85,71 % соответственно. Длительность абстинентного синдрома составляла от 3-5 до 14 дней. Алкогольные изменения личности диагностировались у большинства пациентов: у 30 пациентов основной и у 25 – контрольной групп, 93,75% и 89,29% соответственно.
Социальные последствия алкоголизма (потеря работы, конфликты в семье, развод и т.д.) также имели место в большинстве случаев: у 22 пациентов основной и у 22 – контрольной групп (68,75% и 78,57% соответственно).
У всех больных имелись соматические хронические заболевания, обусловленные длительной интоксикацией алкоголем: чаще других диагностировались алкогольная болезнь печени (хронический токсический стеатогепатит), миокардиодистрофия, артериальная гипертензия. У многих больных выявлялись признаки энцефалопатии, в основном средней степени тяжести, чаще токсического генеза. У всех больных при поступлении выявлялась гиперферментемия, свидетельствующая о токсическом поражении печени.
Таким образом, по возрастным, основным социально-демографическим и клинико-динамическим показателям группы существенно не различались.
В постабстинентном состоянии (период после купирования ААС до 3 – 4-х недель воздержания от употребления алкоголя) у пациентов наиболее частыми были астенические проявления: повышенная утомляемость, вялость, снижение работоспособности. Имели место также различные аффективные нарушения: сниженный фон настроения, тревожность, раздражительность, дисфория, склонность к частой смене настроения, связанные, чаще всего, с обострением патологического влечения к алкоголю. Сохранялись мнестические нарушения, вегетативная дисфункция, расстройства сна (трудности засыпания, поверхностный сон, частые пробуждения).
Этап становления ремиссии (от 4-х недель до 3-х месяцев применительно к данному исследованию) диагностировался при условии, что больной в течение наблюдаемого периода времени полностью воздерживается от употребления алкоголя и других ПАВ.
Основными методами исследования являлись клинико-психопатологический, катамнестический, статистический. Клиническое исследование Цианамида проводилось с использованием специально разработанного протокола, который включал сведения о социальном статусе больных, клинико-динамических характеристиках заболевания, результатах обследования физического и психического состояния, данных лабораторных анализов в динамике. Подробно были представлены сведения об объеме проводимой терапии.
При оценке спектра терапевтической активности препарата использовались специально разработанные в ННЦ наркологии шкалы динамики психопатологических, неврологических, соматовегетативных расстройств в абстинентном состоянии, в постабстинентном периоде, на этапе формирования ремиссии. Оценка безопасности действия препарата производилась с учетом динамики лабораторных показателей (АЛТ, АСТ). Использовалась шкала общего клинического впечатления. На всем протяжении лечения производилась оценка побочных явлений препарата, проводился количественный анализ рецидивов.
Статистическая обработка полученных результатов проводилась в программе SPSS for Windows 11.5, а также Microsoft Excel 2000.
Схема исследования
Лечение было комплексным, включало в ААС проведение стандартных дезинтоксикационных мероприятий, в дополнение к ним в первые 5-7 дней назначались транквилизаторы (реланиум – до 20 мг в сутки, феназепам – до 6 мг в сутки), применялись антиконвульсанты (финлепсин – до 400 мг в сутки). В постабстинентном состоянии и в ремиссии в терапевтических программах применялись антидепрессанты (амитриптилин до 75 мг в сутки, леривон – до 90 мг, ципралекс до 20 мг, ремерон до 30 мг и пр.), дневные транквилизаторы (грандаксин до 150 мг в сутки и др.). При утяжелении состояния, как правило, связанном с актуализацией патологического влечения к алкоголю, назначались нейролептики. Предпочтение отдавалось малым дозам нейролептиков-антипсихотиков (галоперидол до 10 мг, трифтазин до 15 мг, этаперазин до 40 мг, рисполепт до 4 мг), в вечернее время назначались (короткими курсами) препараты с седативным действием (тизерцин до 50 мг, неулептил до 10 мг). Все пациенты получали терапию ноотропами, витаминами, гепатотропами. На всем протяжении стационарного лечения проводилась индивидуальная рациональная психотерапия. Терапевтические схемы были максимально стандартизованы, не отличались по своим подходам в основной и контрольной группах. Различия наблюдались лишь в индивидуальных дозах назначаемых препаратов.
Цианамид назначался в основной группе после купирования явлений ААС на фоне базисной стандартной терапии. В стационарных условиях пациенты принимали препарат по 12 капель (36 мг) 1 раз в день утром. В амбулаторных условиях (этап формирования ремиссии), доза препарата составляла 12 – 25 капель 1 – 2 раза в день (суточная доза 36-75 мг).
В контрольной группе проводилось только базисное лечение. На этапе становления ремиссии пациенты этой группы в ряде случаев получали поддерживающее лечение, но в ее составе не принимали никаких сенсибилизирующих средств.
Результаты исследования
В основной группе исследование продолжили 31 человек, поскольку одному из пациентов в связи с возникшими побочными явлениями (о чем будет сказано позже).
Оценка динамики психопатологических, соматовегетативных и неврологических нарушений у пациентов основной и контрольной групп выявила достоверное снижение степени их выраженности внутри групп в результате проводимого комплексного лечения. При сравнении групп между собой не было обнаружено достоверных различий по указанным параметрам, что свидетельствует о том, что применение Цианамида в комплексных лечебных программах существенно не влияет на динамику психопатологических, соматовегетативных, неврологических проявлений в рамках ААС, постабстинентного состояния, а также на этапе становления ремиссии. Нормализация состояния пациента происходит под влиянием базисной терапии и психотерапевтического воздействия на различных этапах лечения.
В основной группе у 21 пациента (67,74 %) имела место ремиссия на протяжении всего срока исследования. Большинство этих больных (17 человек) прошли исследование без срывов, не отмечалось даже однократного употребления алкоголя. Единичное употребление алкоголя имело место у 4 пациентов основной группы (12,90 %), причем у всех – в течение месяца после выписки (Таблица 1). Употребление алкоголя на фоне приема Цианамида сопровождалось следующими эффектами: спустя 15 – 20 мин. после употребления алкоголя у пациентов появлялись чувство стесненности в груди, одышка, учащенное сердцебиение, перебои в работе сердца, тошнота, рвота, диарея, дрожь, резкое покраснение лица, повышенная потливость, резкая слабость, ощущение распирания в голове, у некоторых резко снижалось АД, появлялась головная боль. Возникали острое чувство страха смерти, тревога, двигательное беспокойство. При этом опасных нарушений со стороны сердечно-сосудистой, пищеварительной, дыхательной, эндокринной систем не отмечалось. Выраженная реакция длилась около часа, указанные расстройства в большинстве случаев не требовали медикаментозной коррекции и в дальнейшем самостоятельно купировались в течение дня (до 12 часов), наиболее длительно сохранялась астеническая симптоматика. После нормализации состояния пациенты на следующий день продолжали прием Цианамида и воздерживались от употребления алкоголя, боясь повторения подобных реакций. Все они вошли в группу лиц с ремиссией.
В 10 случаях в основной группе (32,26 %) был отмечен рецидив заболевания, из них 4 пациента возобновили прием алкоголя в течение месяца после выписки, 2 – на втором месяце и 4 – на третьем месяце амбулаторного лечения. Большинство из них отказывались от приема Цианамида за некоторое время до срыва, при этом, если последний прием Цианамида происходил хотя бы за день до срыва, неприятных явлений не возникало. Несколько пациентов категорически отказывались продолжать прием Цианамида сразу после первой пробы алкоголя на фоне сенсибилизирующей терапии (после ликвидации неприятных ощущений и нормализации состояния продолжали алкоголизироваться). В ряде случаев препарат давали родственники больных без их ведома. Пациенты после срыва ежедневно возобновляли прием алкоголя, невзирая на тяжелые реакции. Нескольким из них требовался вызов скорой медицинской помощи, проводилось симптоматическое лечение. Родные, испугавшись за здоровье пациентов, прекращали терапию Цианамидом, и возникал рецидив заболевания. Эти больные отличались особенно сильным, некорригируемым патологическим влечением к алкоголю, отсутствием инстинкта самосохранения, страха за свое здоровье. Все они имели неоднократные запретительные процедуры и крайне короткие терапевтические ремиссии в анамнезе.
Таблица 1
Количественный анализ рецидивов в основной группе
| Характеристика | Этап становления ремиссии, дни | Всего | |||
| 30 | 60 | 90 | Абс. число | % | |
| Воздержание (ремиссия) | 21 | 21 | 67,74 | ||
| Единичное употребление алкоголя | 4 | 0 | 0 | 4 | 12,90 |
| Рецидив | 4 | 2 | 4 | 10 | 32,26 |
В контрольной группе больше половины пациентов (17 человек – 60,71 %) за время исследования вернулись к употреблению алкоголя. Из них 13 больных возобновили злоупотребление алкоголем в течение месяца (6 – сразу после выписки), 1 – на 2-м месяце, 3 – на третьем месяце амбулаторного лечения. Единичных проб алкоголя в этой группе не наблюдалось, поскольку первая же выпивка приводила к срыву. Воздерживались от употребления алкоголя в течение всего времени исследования 11 пациентов контрольной группы (39,29 %) (таблица 2).
Таблица 2
Количественный анализ рецидивов в контрольной группе
| Характеристика | Этап становления ремиссии, дни | Всего | |||
| 30 | 60 | 90 | Абс. число | % | |
| Воздержание (ремиссия) | 11 | 11 | 39,29 | ||
| Единичное употребление алкоголя | 0 | 0 | 0 | 0 | 0 |
| Рецидив | 13 | 1 | 3 | 17 | 60,71 |
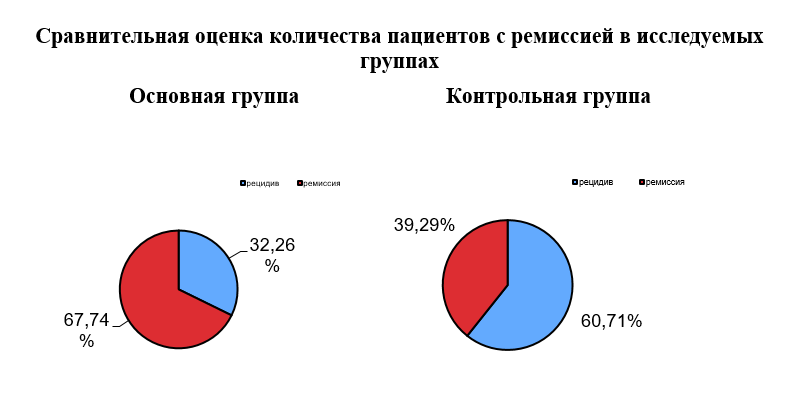
Сравнение качества ремиссий и количества рецидивов в основной и контрольной группах показало достоверно большее количество ремиссий в основной группе (67,74 % в основной и 39,29 % в контрольной, р<0,05), и, соответственно, достоверно меньшее количество рецидивов (рисунок 1). Кроме того, как следует из приведенных выше данных, в контрольной группе большинство пациентов возобновили прием алкоголя в первый же месяц после выписки (рецидив на первом месяце у 13 пациентов, 46,43 %), в то время как в основной группе в течение месяца после выписки рецидив заболевания случился лишь у 2-х пациентов (6,45 %, р<0,05). Единичное употребление алкоголя имел место лишь в основной группе, неприятные явления совместного приема Цианамида и алкоголя заставляли пациентов впоследствии воздерживаться от спиртного, в то время как в контрольной группе отсутствовали сдерживающие факторы, и любое употребление алкоголя приводило к срыву ремиссии.
Рисунок 1
В начале лечения у большинства пациентов имела место гиперферментемия. К концу стационарного курса лечения происходила относительная нормализация показателей АСТ и АЛТ (рисунок 2, 3)
Рисунок 2
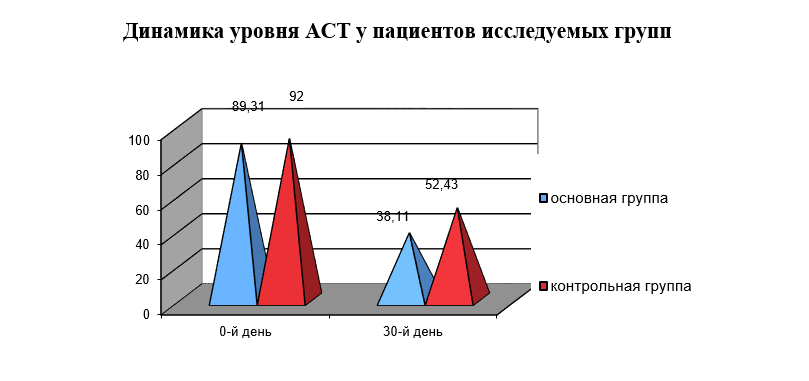
Динамика уровня АСТ у пациентов исследуемых групп
Рисунок 3
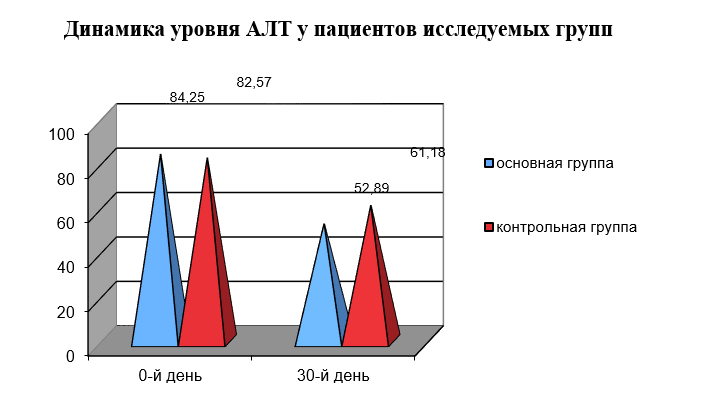
Динамика уровня АЛТ у пациентов исследуемых групп
Как видно из представленных данных, под влиянием комплексного лечения в группах происходило достоверное снижение показателей печеночных ферментов. Таким образом, применение Цианамида не ухудшает функции печени и является безопасным для состояния пациентов.
В ходе лечения у одного пациента основной группы в стационаре на 5-й день приема Цианамида (доза 12 капель однократно утром) возникли побочные явления в виде тошноты, неприятных ощущений в эпигастральной области, которые длились в течение 3–4 часов и прошли самостоятельно, без дополнительной медикаментозной коррекции. В последующие 5 дней пациент продолжал принимать Цианамид, но всякий раз указанные неприятные явления возобновлялись, в связи с чем препарат был заменен на Дисульфирам. У остальных больных при приеме Цианамида практически не возникало осложнений, все они хорошо переносили назначенную терапию.
Выводы
Цианамид показал хорошую эффективность на этапе формирования ремиссии. Применение Цианамида позволило значительно снизить количество ранних рецидивов и, соответственно, улучшить качество ремиссии.
Цианамид хорошо сочетался с психофармакологическими и другими препаратами, не усиливая и не ослабляя их действия, не оказывал угнетающего влияния на психофизическое состояние пациентов. Прием препарата при рекомендуемом режиме дозирования не вызывал ухудшения функций печени или каких либо других значительных побочных эффектов.
Цианамид существенно не влиял на динамику психопатологических, соматовегетативных и неврологических нарушений в структуре постабстинентного состояния и на этапе формирования ремиссии, однако способствовал стабилизации состояния пациентов благодаря улучшению качества ремиссий.
Литература
- Алкоголизм: (Руководство для врачей)/ Под ред. Г.В. Морозова, В.Е. Рожнова, Э.А. Бабаяна. М.: Медицина. 1983.
- Валентик Ю.В., Новиков Е.М. Применение препарата Цианамид при лечении больных алкоголизмом// Наркология. 2002. № 3.
- Ерышев О.Ф. Этапы течения ремиссий при алкоголизме и профилактика рецидивов. Дисс. … д.м.н. в виде научного доклада: СПб. 1998. 58 с.
- Иванец Н.Н., Кинкулькина М.А. Новые данные о сенсибилизирующей терапии алкогольной зависимости // Журнал неврологии и психиатрии им. С.С. Корсакова. 2004. №7. С. 43-48.
- Ajima M., Usuki K., Igarashi A., Okazaki R., Hamano K., Urabe A. and Totsuka Y. Cyanamide-induced granulocytopenia// Internal Medicine. – 1997. – V. 36. – P. 640–642.
- Foster J. H., Peters T. J., Marshall E. J. Quality of life measures and outcome in alcohol-dependent men and women. //Alcohol. – 2000. – Vol. 22, № 1. – P. 45–52.
- Foster J.H., Marshall E.J., Peters T.J. Application of a quality of life measure, the life situation survey (LSS), to alcohol-dependent subjects in relapse and remission. //Alcohol. Clin. Exp. Res. – 2000. – Vol. 24, № 11. – P. 1687–1692.
- Rudolf H., Priebe S. Similarities and differences in subjective quality of life of alcoholic women // Psychiatrische Praxis. — 1999. — Vol. 266, № 3. — P. 116.
- Rudolf H., Priebe S. Subjective quality of life and depressive symptoms in women with alcoholism during detoxification treatment // Drug Alcohol Depend. — 2002. — Vol. 66, № 1. — P. 71–76.
- Suzuki Y., Yokoyama A., Nakano M., Okuyama K., Takahashi H., Tamai H., Maruyama K. and Ishii H. Cyanamide-induced liver dysfunction after abstinence in alcoholics: a long-term follow-up study on four cases// Alcoholism: Clinical and Experimental Research. – 2000. – V. 24. – P. 100S–105S.
- Swift R.M., Flannery B., Roberts A.J., Cooney N., Anton R., Rohsenow D. (2001). The role of craving in alcohol use, dependence, and treatment. Alcohol Clin Exp Res, 25(2), 299-308.
- Swift R. M. Лекарственная терапия алкогольной зависимости // Обзор современной психиатрии. — 2001. — Вып. 3. — С. 61–70.
- Tamai H., Yokoyama A., Okuyama K., Takahashi H., Maruyama K., Suzuki Y. and Ishii H. Comparison of cyanamide and disulfiram in effects on liver function. Alcoholism: Clinical and Experimental Research. – 2000. – V. 24. – P. 97S–99S.
Yokoyama A., Sato S., Maruyama K., Nakano M., Takahashi H., Okuyama K., Takagi T., Yokoyama T. and Hayashida M. (1995) Cyanamide-associated alcoholic liver disease: a sequential histological evaluation. Alcoholism: Clinical and Experimental Research 19, 1307–1311.





